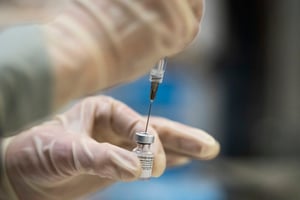
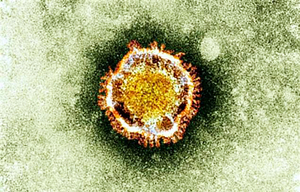
中國科興控股生物技術有限公司研發的「CoronaVac」疫苗完成在巴西的第三期臨床實驗後,原訂12月23日公佈實驗數據,但科興在當日以整合來自全球的臨床試驗數據為由延後15天,這已經是再度延遲。
中國科興控股和巴西生物研究中心布坦坦研究所合作,在巴西聖保羅州進行第三期臨床試驗,有超過一萬人參與。巴西也是全球第一個完成科興疫苗第三期臨床試驗的國家。
不過,原定在12月初發表的巴西科興疫苗實驗數據卻一再延遲公佈,之前在11月24日,已有消息說該研究已經收集到足夠多的感染病例數,將很快公佈中期分析結果。
但直到12月15日,巴西聖保羅州州長又表示,3期臨床數據的公佈要推遲到12月23日,因為這樣可以獲得充份的數據,達到臨床研究的最終點,直接公佈正式的結果。
布坦坦研究所原將在12月23日宣佈該疫苗的有效性,但科興控股又以「分析、整合在印尼和土耳其進行的其它疫苗試驗的結果」為由,要求再延遲15天公佈確切的數據結果。
由於保密合約,布坦坦研究所不能擅自公佈實驗數據,只能透露「CoronaVac」疫苗的保護效力,達到巴西國家衛生監測局所要求的50%以上,並強調推遲發佈確切臨床數據與疫苗的有效性無關。
不過,先前巴西總統波索納洛(Jair Bolsonaro)一再批評中國疫苗研發的過程缺乏公開、透明,此次科興控股又延遲公佈實驗數據,再度引發外界質疑。
美國加州Scripps Research Translational Institute的臨床試驗專家、負責人Eric Topol接受媒體採訪時表示,巴西試驗結果報告欠缺透明度,這是完全不可接受的,而且也不符合美國的相關標準。
早前,巴西的衛生監管機構Anvisa一度宣佈暫停科興生物研發的中共病毒(俗稱武漢病毒、新冠病毒)疫苗的臨床試驗,原因是在10月29日發生「嚴重不良反應」,但沒有提供進一步細節。不過,之後進行試驗的研究所負責人說,死亡與疫苗沒有任何關係。
巴西國家衛生健康監測局(Anvisa)在上周也曾經質疑,中國緊急授權使用克爾來福的標準並不透明。
中國疫苗在國內也遭遇普遍質疑
《南華早報》12月17日報道,中共將在中國新年前,讓5,000萬人接種由中國國藥集團和北京科興公司製造的中共病毒疫苗。目的是為了趕在2月11日開始的新年假期前結束施打,以降低假期間疾病傳播的風險。
「香港01」12月22日發表署名「紀瀾」、題為「國產疫苗首批預計接種5,000萬人次,中國必須講清楚的問題」的評論。評論表示,中國疫苗實驗數據至今未曾公佈,臨床試驗剛展開就投入緊急使用,有待中方釋疑。中國才剛開始啟動三期臨床試驗幾天,就開始緊急使用,疫苗可供接種的數據來源何在?
英國《金融時報》16日刊登的題為《中國疫苗走向世界需解決的問題》的時事分析,現在中國研製的疫苗中,不僅沒有一款走完研製疫苗應該走的所有程序,有的疫苗連第一階段動物實驗的數據都沒有公佈即進入人體臨床試驗階段,後續恐出現問題,
《大紀元》獲悉,上海楊浦中醫醫院11月末做了一次摸底調查,逾九成醫護人員拒絕接種國產疫苗。
網上還傳出中共政府部門聊天群組截圖,儘管官方發出「緊急通知」,但政府部門無一人報名接受「免費接種」疫苗。
12月22日,大陸華山醫院感染科主任張文宏的一段「讓領導幹部先打」的影片在網絡熱傳。#
-------------------
局勢持續演變
與您見證世界格局重塑
-------------------
🔔下載大紀元App 接收即時新聞通知:
🍎iOS:https://bit.ly/epochhkios
🤖Android:https://bit.ly/epochhkand
📰周末版實體報銷售點👇🏻
http://epochtimeshk.org/stores