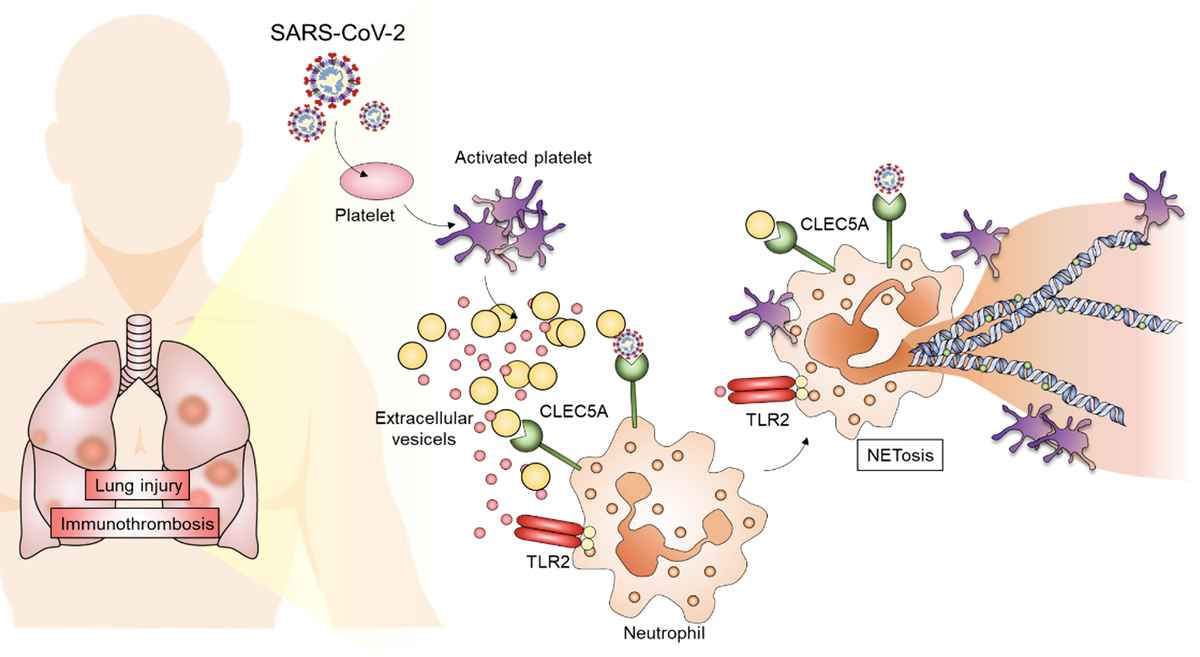
感染COVID-19會導致肺臟內形成血栓,嚴重時可能致命,也有引發嚴重後遺症的風險。台灣中研院一項研究發現COVID-19患者發生血栓的關鍵原因,COVID-19病原體SARS-CoV-2會活化血小板以放大發炎反應,進而產生血栓。只要阻斷嗜中性白血球表面的兩個受體CLEC5A和TLR2,就可以緩解血栓症狀並且減少血管內凝血以及發炎。
研究報告的第一作者、基因體研究中心博士後研究學者宋佩珊表示,收集COVID-19急性期患者的血液樣本發現,血液中含有高量的胞外囊泡(EV),這些囊泡大多來自血小板,顯然與血小板遭遇病毒之後被活化有關。當血小板被病毒激活後,釋放大量胞外囊體刺激嗜中性白血球,產生大量的嗜中性白血球胞外網狀結構(NETs)及自殺式細胞死亡(NETosis)。早前研究已經發現,雖然NETs形成有助於清除病菌,但過多NETs會引發血栓,導致肺部微血管阻塞。
研究團隊分別採取健康受試者、COVID-19病人的胞外囊泡進行質譜儀分析,發現,SARS-CoV-2感染引起的胞外囊泡表現大量血小板相關蛋白,且具有多種與白血球去顆粒性及血小板活化凝集的蛋白,顯示COVID-19病人血液中血小板劇烈活化。
研究團隊進一步將健康人和COVID-19病人的胞外囊泡與嗜中性白血球培養,結果顯示健康對照組的胞外囊泡無法誘導NETs形成,但COVID-19病人的胞外囊泡誘導了強大的NETs形成,而阻斷嗜中性白血球表面的兩個受體CLEC5A和TLR2,能夠抑制NETs形成。
在動物實驗中,研究人員發現,小鼠感染SARS-CoV-2病毒3至5天後,肺部會產生大量的NETs以及嚴重的細胞浸潤;而對於CLEC5A和TLR2基因剔除的小鼠,發炎以及細胞浸潤的情況大幅降低。
中研院基因體研究中心特聘研究員謝世良指出,CLEC5A和TLR2是有希望的治療靶點,可在未來減輕血栓炎症,並降低產生COVID-19後遺症的風險。
研究已發表在《Journal of Biomedical Science》期刊。@
------------------
🎥【動紀元】每日有片你睇:
https://bit.ly/3PJu3tg
☑️ 登記會員享專屬服務:
https://hk.epochtimes.com/subscribe
☑️ 贊助大紀元:
https://www.epochtimeshk.org/sponsors
☑️ 成為我們的Patron:
https://www.patreon.com/epochtimeshk
-------------------
局勢持續演變
與您見證世界格局重塑
-------------------
🔔下載大紀元App 接收即時新聞通知:
🍎iOS:https://bit.ly/epochhkios
🤖Android:https://bit.ly/epochhkand
📰周末版實體報銷售點👇🏻
http://epochtimeshk.org/stores