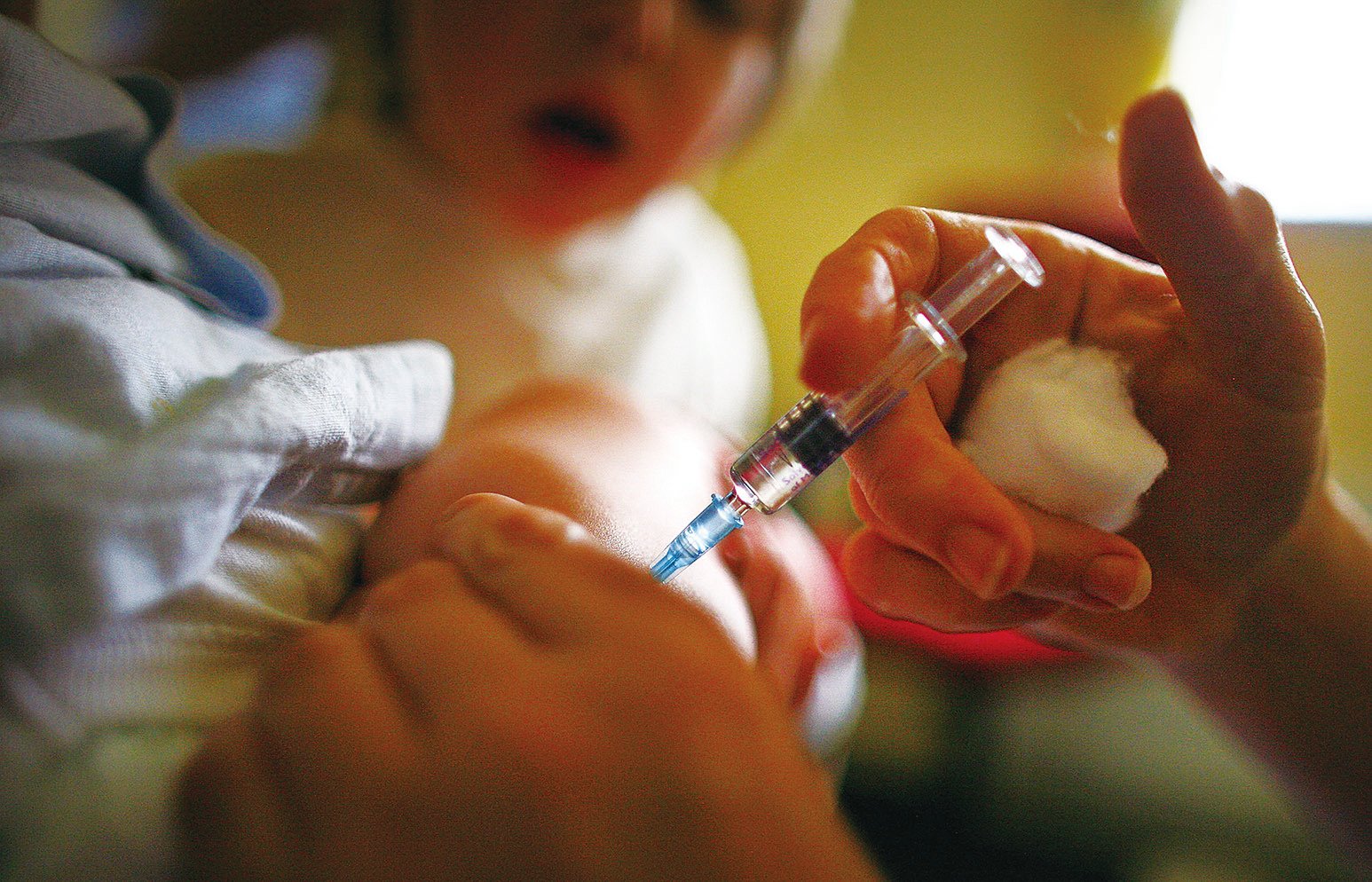
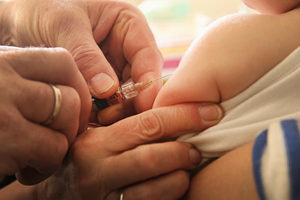
國產長生生物疫苗造假事件,令中國大陸眾多恐慌的家長將眼光投向了進口疫苗。然而,進口疫苗並非想打就能打。微信公號「浪潮工作室」近日發文《我們為甚麼打不上進口疫苗》剖析了其中的原因。
作為人口第一大國,人用疫苗又是一個相當剛需的產品,因而用戶數量巨大的中國市場一直是外資疫苗企業青睞的「潛力股」。但進入中國市場卻非易事。
門檻高到讓人無法理解
文章說,中國擁有據說是「全世界最嚴格」的疫苗監督體系,除了臨床試驗外,還要經過1至5年不等的評審時間,才能頒發《進口藥品註冊證》。而且中國對進口疫苗的評審標準,有時候高到讓人無法理解的程度。
以宮頸癌疫苗為例。它於2006年在美國上市,此後迅速在全球100多個國家和地區(包括香港、澳門和台灣)被批准使用,然而,大陸地區卻拖了整整十年,才同意讓宮頸癌疫苗進入。
對久拖未決的原因,文章表示,雖然子宮頸癌疫苗能夠預防HPV(人乳頭瘤病毒)感染、而且HPV感染早被證實可以導致子宮頸癌,但是中國食藥監(CFDA)卻堅持認為,這兩個事實無法推導出「子宮頸癌疫苗可以降低子宮頸癌發病率」的結論。要求申請者花上更長時間,蒐集直接致病數據才行。
這種與全球其它國家地區格格不入的標準,讓許多女性錯過了打疫苗的最佳時機。
此外,即使進口疫苗拿到了上述的註冊許可,也並不代表可以高枕無憂,因為進口許可證需要5年續期一次,一不小心,就會前功盡棄。
2015年4月,輝瑞因進口許可證過期後續期被拒,宣佈停供沛兒7價肺炎疫苗。而當時更先進的沛兒13價還在緩慢審批中,沛兒7價是國內唯一肺炎疫苗,無替代品。CFDA沒透露為何拒絕輝瑞的續期申請。有分析指,這或是想為國內肺炎疫苗研發爭取時間。
文章認為,CFDA想不惜代價保護國內疫苗企業,而普通民眾都可能成為那個代價。
這次事件造成了全國性的、持續三年的肺炎疫苗斷檔。不少孩子已經打過一針、兩針,最後家長被告知疫苗已經斷貨,原本制定好的後續打針計劃,就只能這樣胎死腹中。
另外,進口疫苗不僅要拿到藥品註冊許可,還要符合《中國藥典》的要求。
文章說,《藥典》每隔5年就修訂一次,假如不符合新版藥典的要求,那麼即使疫苗已經通過其他所有審批、在中國安全銷售了很久,也必須下架。
2010年10月,新版的藥典對疫苗中Vero細胞DNA殘留量等提出了更高的要求,不少進口疫苗只能打包袱滾回家。
每年進口疫苗批簽發的數量佔所有疫苗的不到10%,2011年,受新版藥典影響,進口疫苗的數量狂跌到了4%。
國產疫苗質遠不如印度
那麼,疫苗准入門檻高,是否意味著國產疫苗質量會優於進口疫苗呢?
文章分析,中國從來就不是疫苗發達國家,防疫水平也還處在初級階段,目前只對甲類和乙類傳染性疾病中的大多數有比較穩定的控制,對丙類傳染性疾病的控制能力還很低。雖然中國擁有38家疫苗生產企業,數量全球第一,但疫苗質量卻遠遠落後於印度。
國內的疫苗企業缺乏自主創新能力,名牌產品極少,市場競爭力很低。而國產疫苗總體在穩定性、產能及關鍵技術上,與進口疫苗相比還有一定的差距。
文章表示,聯合國兒童基金會每年都要代表數十個貧窮國家進行疫苗大批的採購。為壓縮預算,有40%的疫苗(約12億支)要從發展中國家的廠家那裏買。而印度基本包攬了這些訂單。
因為為了保證疫苗的質量,只有通過了WHO預認證的疫苗,才有資格參加聯合國機構的採購。
想要讓疫苗通過這個WHO預認證,首先,生產該疫苗的國家必須先通過世衛組織的國家監管體系評估。換句話說,世衛的國家監管體系評估只是一個最基本的標準。從1999年起,中國就開始申請這個評估了,不及格了兩次,一直到2011年,才成為第36個通過這個評估的國家。
要知道,據世界衛生組織(WHO)的統計,全球只有48個國家生產疫苗,而且其中只有27個國家是常規生產大量疫苗的。
早在2006年,印度就已經有7個品種的疫苗通過了WHO預認證,而中國直到2013年,才第一次有疫苗(成都所的乙腦疫苗)通過WHO預認證。
也就是說,中國大陸生產的大部份疫苗,連出口去援助最貧窮國家的資格都沒有。目前中國總共有4個疫苗品種通過預認證,而印度已經有40多個了。
文章認為,CFDA對進口疫苗的苛刻要求,與其說是為人民健康著想,不如說是對國產疫苗的「護短」式保護政策。◇
-------------------
局勢持續演變
與您見證世界格局重塑
-------------------
🔔下載大紀元App 接收即時新聞通知:
🍎iOS:https://bit.ly/epochhkios
🤖Android:https://bit.ly/epochhkand
📰周末版實體報銷售點👇🏻
http://epochtimeshk.org/stores