最新臨床發現,一種在研的治療伊波拉病毒藥物迅速緩解了一名新型冠狀病毒患者的嚴重肺炎症狀。《紐英倫醫學雜誌》(NEJM)周五(1月31日)發表了一篇介紹美國首例確診新型冠狀病毒病例的診療過程以及臨床表現的報告,其中提到這一點。
源自中國武漢的新型冠狀病毒已經蔓延到世界多個國家和地區,而公開治療臨床信息無論是對大眾了解最新的疾病特徵,或者指導醫護人員診療都有著重要的作用。本文將介紹美國首例新型冠狀病毒病例的臨床康復紀錄。
2月3日,華盛頓州埃弗里特普羅維登斯地區醫療中心宣佈,美國首例新型冠病毒病人在接受治療後已經出院。目前,他正在家裏自我隔離,並在康復中。
病毒患者是一名35歲來自中國的男性,1月15日從武漢探親返美,隨後四天出現咳嗽以及發熱症狀。因為之前有看過美國疾病與預防中心(CDC)關於新型冠狀病毒的健康警報,患者結合自己的症狀和武漢旅行史後決定去看醫生。
1月19日,患者前往位於華盛頓州斯諾霍米什(Snohomish,位於西雅圖北邊約45分鐘車程)郡的一家急症室。患者沒有到過華南海鮮市場,也沒有和確診病人接觸過。
初步診斷結果
在急症室,醫生們獲得患者的第一批生理數據。體溫為37.2度,肺部有聽診音。然而,X光胸片結果沒有異常。
醫務人員也收集了他的鼻咽拭子樣本,用於病原體的檢驗,而甲流和乙流的檢驗結果均為陰性。醫生們同樣也沒有檢測出副流感、呼吸道合胞病毒、鼻病毒,以及腺病毒的存在。此外,醫生們還檢測了4種已知能感染人類,導致疾病的常見冠狀病毒(HKU1,NL63,229E,OC43),結果仍然是陰性。
基於患者的武漢旅行史,當地以及州衛生部門決定即可將此病例通知聯邦機構——美國疾病管制與預防中心(Centers for Disease Control and Prevention,簡稱CDC),CDC很快決定檢測這名患者是否攜帶新型冠狀病毒,隨後患者在當地衛生部門的監督下在家進行自我隔離。
1月20日,檢測結果返回:該患者的鼻咽拭子和口咽拭子樣本,均呈現新型冠狀病毒陽性。於是,這名患者被收治於西雅圖附近一家醫院的隔離病房進行治療。
住院後早期治療無異樣
患者在住院時,已出現噁心和嘔吐現象,同時也有持續發燒和乾咳,但沒有氣短或胸痛,主要生理指標也在正常範圍之內。因此,最初這名患者只是接受輔助性的照料,包括每天輸注2升生理鹽水,並接受恩丹西酮的治療,以緩解噁心。
在接下來的5天裏,除了伴有心動過速的高燒之外,這名患者的主要生理指標依舊維持穩定。在住院第2天(患病第6天),他出現了腹瀉和腹部不適。值得一提的是,在腹瀉的糞便樣本中,也檢測出了新型冠狀病毒(rRT-PCR結果陽性)。總體來說,住院前幾天,治療以輔助性為主,以協助患者控制症狀。
病情惡化 發展為嚴重肺炎
在住院第3天(患病第7天),患者的X光胸片看起來依舊沒有異常。然而到了住院第5天(患病第9天),左肺下葉出現了肺炎的特徵。在出現肺炎特徵的同一天晚上,患者的呼吸情況也有所變化,氧飽和度下降到了90%。
住院第6天(患病第10天),醫生們決定為患者輸氧。考慮到病情的惡化,以及擔心患者出現獲得性肺炎,醫生們開始使用萬古黴素和頭孢吡肟兩種抗生素進行治療。
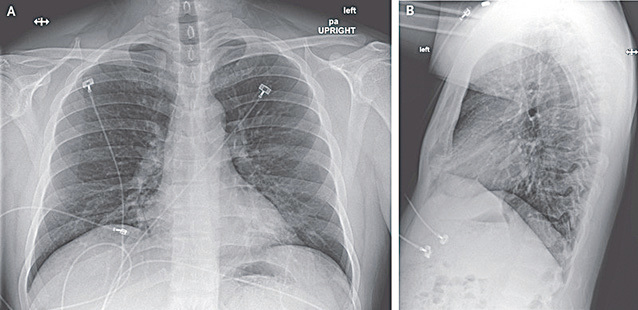
當天的患者X光胸片結果顯示出沙士的特徵,兩側肺部都有基底條紋狀的混濁物。
同時,患者出現持續高燒,多個部位的樣本檢測出新型冠狀病毒,並發展成為嚴重肺炎。使用抗伊波拉的藥物治療 病情快速緩解
住院第7天(患病第11天),醫生們決定為患者提供一種正在研發中的新型藥物——由吉利德(Gilead)公司研發的抗病藥物瑞德西韋(Remdesivir)——一種核甘酸類似物前藥,能夠抑制依賴RNA的RNA合成酶(RdRp)。
這種在研療法本是計劃用於治療埃博拉病毒,不過因為埃博拉病毒也同樣有RdRp。因此,這種在研療法也有望對冠狀病毒進行抑制。
《科學》雜誌也曾在1月27日的報道中指出,最有潛力的抗新型冠狀病毒藥物可能是抗埃博拉病毒藥物瑞德西韋。
在住院第7天晚上,這名患者接受了瑞德西韋的靜脈輸注。
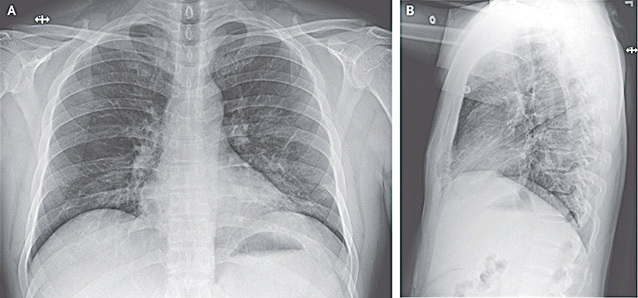
住院第8天(患病第12天),這名患者的臨床症狀出現了立竿見影的改善。他不再需要吸氧,氧飽和度也恢復到了94%~96%。除了乾咳和流鼻涕外,他已沒有其它症狀。同時,患者的食慾也得到改善。
截至1月30日,患者雖仍在住院觀察,但已退燒。唯一的症狀就是咳嗽,但程度正在逐日減緩。
研究者的最新發現與討論
在論文的討論環節,作者指出在這名患者患病的第4天和第7天的檢測結果表明,病毒具有很高的載量水平以及傳播潛力。同時,糞便檢測出現的新型冠狀病毒陽性也值得注意。此外,患者血清標本有多次反覆出現陰性,這一點跟中國重症患者血液中檢測出病毒不一致。
作者還指出,目前對新型冠狀病毒的臨床了解仍非常有限。中國報告的併發症已經包括:嚴重肺炎、呼吸衰竭、急性呼吸窘迫綜合徵和心臟損傷等。
「但是,需要重點指出,這些病例是在(中國患者)他們的肺炎診斷基礎上識別的,因此可能會使報告偏向更嚴重的結果。」文章寫道。
文章還表示,從美國的首例臨床患者來看,早期他只有發燒和咳嗽的現象,直到症狀出現的第九天,病情才發展到肺炎階段。考慮到早期的症狀非常輕微,且和其它冬季的傳染性疾病有著類似之處,這也增加了診斷的難度。
換句話說,新型冠狀病毒患者的前期臨床表現可能遠比中國報告的症狀要輕,而且很可能有疑似病例被忽略或被錯誤識別。
抗病藥物仍需臨床對照試驗才能確保安全與有效
至於大眾關心的抗病藥物瑞德西韋,論文作者認為,這是基於患者病情惡化,遵循美國「同情用藥」(compassionate use)原則進行的治療。儘管在治療之後,患者病情出現了迅速緩解,但依然需要進行隨機對照的臨床試驗,來確定藥物瑞德西韋以及其它在研藥物在治療新型冠狀病毒感染上的安全性和有效性。
瑞德西韋為吉利德公司的在研藥物,尚未在全球任何地方獲得許可或批准。
吉利德(Gilead)公司周五聲明,「瑞德西韋已在動物模型中證明了對MERS和SARS病毒病原體有體外和體內活性,這兩者的病毒病原體與新型冠狀病毒具有結構上的相似之處。」在沒有獲得各國監管當局的批准情況下,吉利德只給少數新型冠狀病毒患者提供瑞德西韋的緊急治療。
吉利德日前表示,正在與美國和中國的研究人員和臨床醫生就新型冠狀病毒進行積極溝通,並討論使用在研藥物瑞德西韋進行治療的可能性。
吉利德公司承諾將在適當的情況下提供瑞德西韋,用於同情用藥及對照的臨床試驗,以支持有效及時地應對類似埃博拉病毒、其它絲狀病毒和病毒病原體感染等全球範圍內的病毒感染疫情。
吉利德是一家以研究為基礎,從事藥品開發和銷售的生物製藥公司,其產品領域主要包括愛滋病、肝臟疾病、癌症、炎症和呼吸系統疾病以及心血管疾病。◇
-------------------
局勢持續演變
與您見證世界格局重塑
-------------------
🔔下載大紀元App 接收即時新聞通知:
🍎iOS:https://bit.ly/epochhkios
🤖Android:https://bit.ly/epochhkand
📰周末版實體報銷售點👇🏻
http://epochtimeshk.org/stores